In Italia sono più di 3 milioni di persone a soffrire di disfunzione tiroidea, con significativa prevalenza delle donne. In questo articolo si descriveranno l’iper e l’ipotiroidismo, la funzione della tiroide ed infine si porteranno alla luce i possibili effetti negativi di una terapia ormonale sostitutiva non necessaria con levotiroxina.
Non è facile individuare una disfunzione alla tiroide, poiché i sintomi sono diversi a seconda della tipologia del disturbo. Questi sintomi sono, in generale, agli antipodi quelli che contraddistinguono l’ipotiroidismo dall’ipertiroidismo, spesso di lieve entità e poco specifici: per questo si stima che oltre il 50% delle persone che ha disfunzioni tiroidee non lo sappia, non si rivolge al medico e, quando lo fa, non riceve una diagnosi corretta e tempestiva. Con il passare del tempo, se non curata con la terapia appropriata, la disfunzione può peggiorare, con impatti significativi sulla salute e sulla qualità della vita.
Tiroide e ormoni tiroidei
La tiroide è una ghiandola a forma di farfalla, posizionata nella regione anteriore del collo (Fig.1). È costituita da due lobi, destro e sinistro, uniti da uno stretto ponte che prende il nome di istmo.
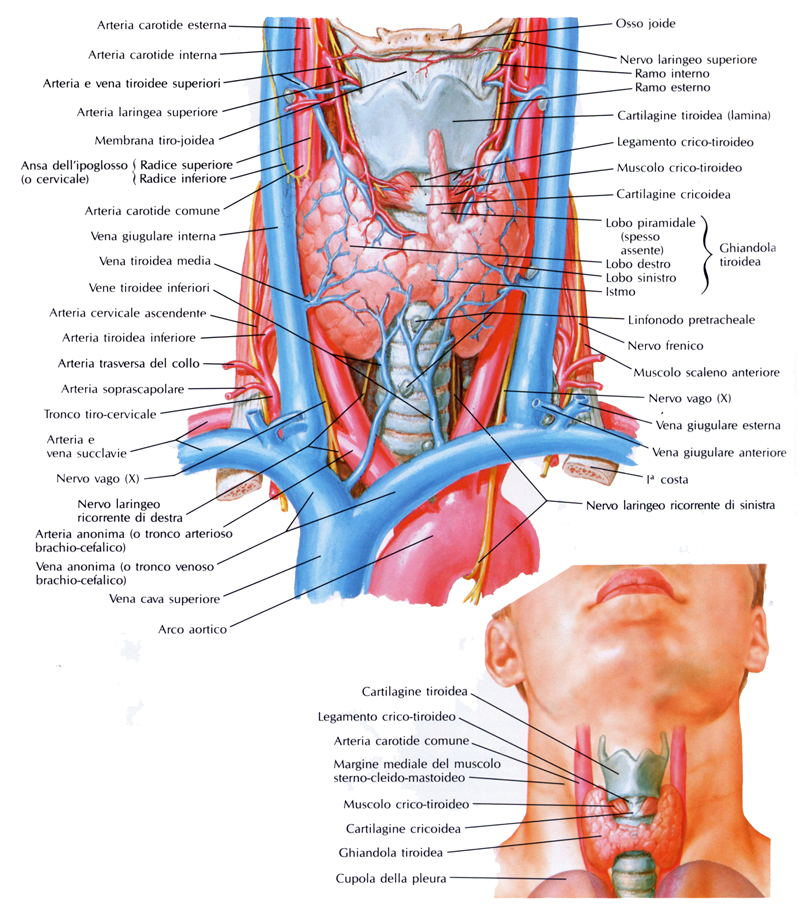
Fig.1 – Posizione anatomica della tiroide
La ghiandola è formata da numerose unità strutturali denominate follicoli. Ciascuno di questi follicoli è un piccolo sacco chiuso tappezzato da uno strato di cellule che circoscrivono una cavità centrale. La colloide è la sostanza che riempie questi piccoli spazi, ed è costituita prevalentemente da tireoglobulina, una proteina contenente iodio.
Le cellule della tiroide sono specializzate per catturare lo iodio presente nel sangue, sotto forma di ione ioduro (I–). Lo iodio catturato viene utilizzato dalle cellule follicolari per iodinare la tirosina ed avviare la produzione dell’ormone tiroideo.
L’ormone tiroideo è composto a sua volta da due ormoni: la tiroxina (tetraiodotironina o T4) e la triiodotironina (T3). Questi due ormoni si combinano all’interno del follicolo tiroideo per formare la proteina tireoglobulina.
Il rilascio di questi ormoni immagazzinati all’interno della tiroide è regolato dal sistema endocrino dell’organismo, in particolare l’ormone TRH (ormone di rilascio della tireotropina), liberato dall’ipotalamo, provoca il rilascio a sua volta da parte dall’ipofisi dell’ormone TSH o tireotropina (ormone stimolante la tiroide) che agisce sui recettori di membrana delle cellule follicolari della tiroide provocando l’immissione nella circolazione sanguigna degli ormoni T3 e T4.
Gli ormoni tiroidei T3 e T4 agiscono direttamente nel nucleo delle cellule bersaglio dell’organismo, modificandone l’espressione genica; in particolare si comportano come repressori del gene bersaglio.
Gli effetti fisiologici degli ormoni tiroidei si dividono in due categorie: quelli che interessano il metabolismo e quelli che interessano crescita e sviluppo.
Effetti sul metabolismo: gli ormoni tiroidei inducono un aumento del metabolismo dei carboidrati, dei grassi e delle proteine. La maggior parte di questi effetti è prodotta in associazione con altri ormoni, come l’insulina, il glucagone, i glucocorticoidi e le catecolamine. Si verifica un aumento nel consumo di ossigeno e nella produzione di calore che si manifesta come aumento del metabolismo basale. Ciò riflette l’azione di questi ormoni sul cuore, rene, fegato e milza. L’azione termogenica è un’importante componente della risposta al freddo ambientale.
Effetti su crescita e sviluppo: gli ormoni tiroidei svolgono un ruolo fondamentale nella crescita, in parte grazie all’azione diretta alle cellule, ed in parte indirettamente, influenzando la produzione dell’ormone della crescita e potenziandone gli effetti sui tessuti bersaglio. Gli ormoni tiroidei sono importanti per una risposta normale al paratormone ed alla calcitonina e per lo sviluppo del sistema osseo. Sono anche particolarmente necessari per lo sviluppo e la maturazione del sistema nervoso centrale. La carenza di ormoni tiroidei durante la vita fetale e neonatale porta a gravi e permanenti ritardi dello sviluppo neurologico e scheletrico del bambino. Tale ritardo è noto con il nome di cretinismo, che può essere prevenuto con la somministrazione di iodio alla madre.
Ipertiroidismo e ipotiroidismo
Ipertiroidismo: è una condizione patologica di esagerata attività funzionale della tiroide con presenza in circolo di una quantità elevata di ormoni tiroidei. Questi sono responsabili di sintomi in parte direttamente (dimagrimento, aumento della temperatura corporea) ed in parte agendo con altri sistemi catecolaminergici (tremori, tachicardia, sudorazione, diarrea). Il quadro sintomatico dell’ipertiroidismo è noto come tireotossicosi.
Nella maggioranza dei casi la tireotossicosi è causata dal morbo di Graves, seguito dal gozzo nodulare tossico (20% dei casi) e dall’adenoma tossico (10% dei casi). In una piccola percentuale di casi può essere la conseguenza di varie forme di tiroidite, di causa iatrogena (errori di dosaggio della terapia sostitutiva o somministrazioni improprie a scopo dimagrante), o fittizie (assunzione volontaria di ormoni tiroidei per sfruttare l’effetto euforizzante), oppure dell’assunzione di eccessive quantità di iodio (Jod-Basedow).
L’entità dei danni al corpo causati da tireotossicosi è estremamente variabile: si passa da danni anche molto gravi ai tessuti con pericolo di vita per il paziente (morte per insufficienza cardiaca), a casi di tireotossicosi subclinica.
I principali sintomi dell’ipertiroidismo coinvolgono il sistema cardiaco e si manifestano con ipercinesie (palpitazioni, tachicardia, fibrillazione atriale, soffi), ipertensione sistolica, polso ampio (aumentata differenza tra pressione massima e minima). Nel paziente anziano o cardiopatico la tireotossicosi può precipitare in un’insufficienza cardiaca o crisi anginose. Diversi sintomi si manifestano a carico del sistema nervoso centrale, quali iperattività, irritabilità, insonnia, incapacità a concentrarsi, tremori alle mani, iperriflessia). Altri sintomi sono perdita di peso, intolleranza al caldo, aumento della sudorazione, atrofia muscolare, retrazione delle palpebre.
Ipotiroidismo: le più importanti cause di ipotiroidismo sono: insufficienza funzionale della tiroide da tiroiditi autoimmuni (tiroidite di Hashimoto e tiroidite atrofica), carenza di iodio nella dieta, terapia con iodio radioattivo, rimozione della tiroide, utilizzo di farmaci antitiroidei o a base di litio (per la cura di disturbi di tipo psichiatrico) ed ipofunzione dell’ipofisi o dell’ipotalamo. Tuttavia l’ipotiroidismo con gozzo da carenza di iodio rimane la più frequente causa di malattia tiroidea a livello mondiale.
La gravità dell’ipotiroidismo è molto variabile (da asintomatico a manifesto con alterazioni della funzione di uno o più organi), ma raramente è tale da costituire un’emergenza medica.
I segni clinici dell’ipotiroidismo riguardano l’alterazione della funzionalità di numerosi sistemi e rappresentano di solito variazioni in senso opposto a quelle dell’ipertiroidismo. Fra i più caratteristici: debolezza, letargia, rallentamento dei movimenti, riduzione della capacità di attenzione, intolleranza al freddo, bradicardia, voce roca, scarso appetito, costipazione, secchezza dei capelli e della pelle, diminuzione della libido e disturbi mestruali.
Il fabbisogno quotidiano pro capite di iodio è di 50 mg; la carenza di iodio nel terreno di alcune aree geografiche e nell’acqua porta al consumo di alimenti a scarso contenuto di tale minerale. La carenza iodica coinvolge probabilmente circa 200 milioni di persone nel mondo, particolarmente colpite sono aree come catena delle Ande, Himalaya ed ampie aree del Sud America e Asia.
Il rischio di sviluppare ipotiroidismo aumenta con l’avanzare dell’età e questa patologia colpisce prevalentemente il sesso femminile.
L’ipotiroidismo subclinico è una condizione patologica in cui l’aumento progressivo della produzione dell’ormone TSH non è accompagnato da appropriata stimolazione tiroidea a liberare il T3 ed il T4, come avverrebbe in condizioni normali. Si instaura quindi una sorta di “resistenza” al TSH da parte della tiroide. L’ipotiroidismo subclinico generalmente è asintomatico e sovente può sfociare in ipotiroidismo conclamato in cui si manifestano i tipici sintomi.
Levotiroxina, attenzione all’utilizzo di questo farmaco!
L’unico trattamento efficace dell’ipotiroidismo, eccetto il caso in cui è dovuto ad una carenza di iodio, è la somministrazione orale degli ormoni tiroidei.
Chiunque soffra di ipotiroidismo sa quanto la qualità della sua vita sia legata all’assunzione della pillola giornaliera a base dilevotiroxina. Questo farmaco è disponibile in commercio con i nomi Eutirox® o Tirosint® a dosaggi che variano dai 25 microgrammi al giorno ai 200 microgrammi giornalieri.
Il farmaco penetra nel corpo ed agisce come un vero e proprio ormone tiroideo, attivando i medesimi meccanismi fisiologici degli ormoni tiroxina (tetraiodotironina o T4) e triodotironina (T3).
La produzione ed il rilascio degli ormoni T3 e T4 variano durante la vita delle persone e durante il giorno, infatti maggiori quantità di ormoni tiroidei vengono rilasciati nelle ore serali e durante la notte piuttosto che nelle ore diurne, di conseguenza gli effetti del farmaco tiroxina si sommano a quelli degli ormoni endogeni.
Spesso si assume levotiroxina a dosi troppo elevate o troppo a lungo, quando non c’è alcuna necessità o vantaggio clinico, senza considerare l’attività degli ormoni tiroidei endogeni e la variabilità delle loro concentrazioni nel sangue durante il giorno e nel corso degli anni. Un utilizzo cronico di levotiroxina è infatti associato ad una perdita di massa ossea (che può provocare osteoporosi) ed all’instaurarsi di aritmie cardiache, fattori di rischio per l’ictus cerebrale.

